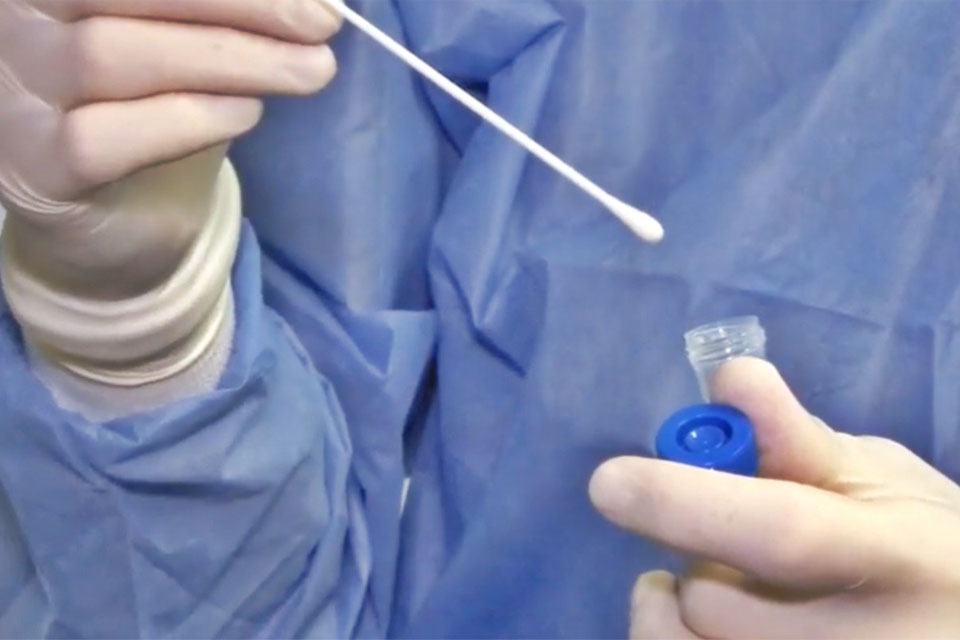
LaAdministración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat)aprobó el uso individual de cuatro test de autoevaluación en base a ladetección del
Losmismos pertenecen a los laboratorios Abbott, Roche, Vyam Group y Wiener, deventa exclusiva en farmacias.
Segúninformó el Ministerio de Salud mediante un comunicado, el resultado de laprueba de orientación diagnóstica debe reportarse de manera individualizadadentro de las 24 horas de realizado el test, informó el Ministerio de Salud enun comunicado.
Los productos aprobados por la Anmatson Panbio COVID-19 Antigen Self-Test, SARS-CoV-2 Antigen Self Test Nasal,SARS-CoV-2 Antigen Rapid Test (COVID-19 Ag) y WL Check SARS-CoV-2 Ag SelfTesting,
Telamcomunicó que los mencionados controles que son de orientación diagnóstica y losusuarios deben recoger la muestra por sí mismos de acuerdo las instrucciones delos fabricantes.
Ladecisión se tomó basándose en la documentación presentada y a partir del consensosurgido en las reuniones del Consejo Federal de Salud (Cofesa) y de lasolicitud del sector privado
Estocon el objetivo de sumar herramientas de autocuidado en el marco de la pandemiade coronavirus, que en la actualidad presenta un incremento en la curva decontagios en nuestro país.
Caberecordar que la aprobación de estos autotest llega luego del reclamo dediferentes funcionarios, como el diputado nacional entrerriano, de Juntos porel Cambio, Pedro Galimberti.
Lostest de autoevaluación para la detección de SARS-CoV-2 (Covid-19) se podránadquirirse en forma individual, por instituciones públicas o privadas, o através de jurisdicciones, en la medida que se garantice el adecuado reporte deresultados.
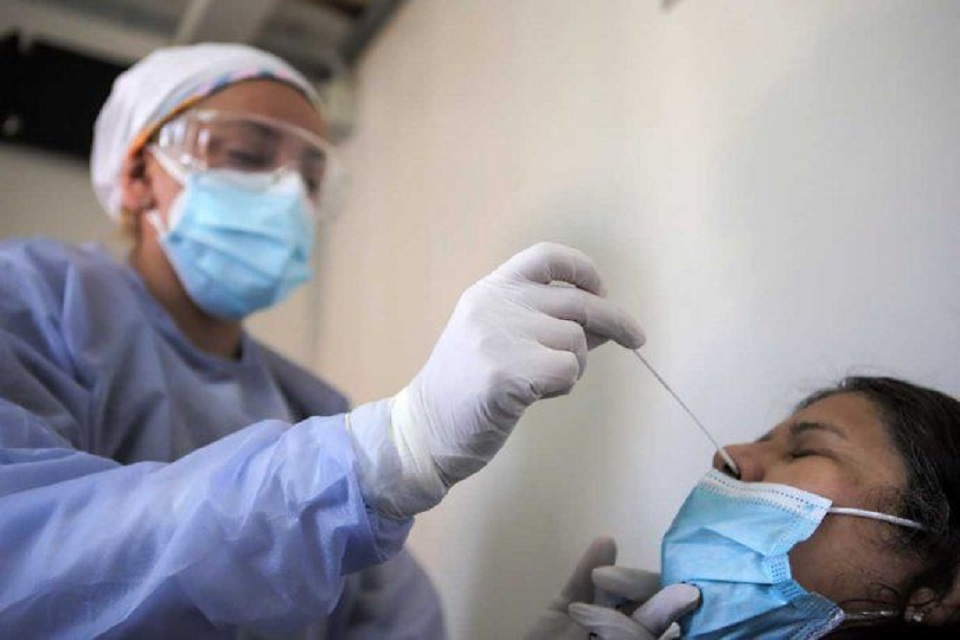
Estas pruebas proporcionan resultados sin valor diagnóstico concluyente señaló la Anmat.
“Estaspruebas proporcionan resultados orientativos, sin valor diagnósticoconcluyente, a excepción de que las jurisdicciones, en acuerdo con elMinisterio de Salud de la Nación y en base a la situación epidemiológica,consideren el resultado como positivo”, aclaró la Anmat en un comunicado.
Allímismo, el organismo explicó que en estos test la muestra se realiza a nivelnasal o bien por saliva, según lo que especifique el fabricante
Eneste aspecto se diferencia de los controles de uso profesional donde la toma demuestra es a nivel nasofaríngeo.
Porello se reforzó que la muestra debe tomarse correctamente y que de inmediato serealice la prueba para evitar resultados erróneos.
Otropunto especificado por la Administración Nacional de Medicamentos, Alimentos yTecnología Médica fue que un resultado negativo de estas pruebas no descarta lainfección.
“Sila persona no tiene síntomas o si la carga viral es baja (lo que puede ocurrirdurante los días iniciales o finales de la infección) el SARS-CoV-2 puede serno detectado por el test”, expresaron.
“Paratener un seguimiento, los resultados deberán ser reportados de forma inmediata(en base al código de barra de cada empaque) una vez realizado el test, y sedispondrá de un plazo mayor cuando no hubiera sido utilizado, ya sea por elusuario individual o por un responsable de reporte en caso de gran volumen detest”, anunciaron desde la cartera de Salud.
Los productos pertenecen a los laboratorios Abbott, Roche, Vyam Group y Wiener
Asu vez, los datos que se vayan reportando serán alojados en la base informáticafarmacéutica, y correspondientemente informados al Sistema Nacional deVigilancia de la Salud (SNVS) por las agrupaciones farmacéuticas habilitadas,en el caso de reporte de test de usuarios individuales o por institucionespúblicas o privadas.
Una vez realizado el test, losresultados deberán reportarse de forma inmediata.
Entanto que, los casos positivos se integrarán a la notificación de casos deCovid-19, mientras que los negativos serán clasificados como “negativo, sinclasificar”.
Finalmente,los casos de test inválido deberán repetirse para definir el resultado.
Siel farmacéutico no recibe el reporte del usuario una vez realizado el test,deberá informar de esa situación a la autoridad sanitaria jurisdiccional.
?? La escalada de casos de COVID hace necesario la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) evalúe con premura la autorización de autotest domiciliarios, de bajo costo, que estén disponibles en farmacias.
— Pedro Galimberti (@pjgalimberti) January 5, 2022
LaAnmat consignó que esta herramienta fue implementada como test deautoevaluación desde el año pasado por países como Portugal, Francia, PaísesBajos, Bélgica, Reino Unido, Italia, Alemania, España, Austria, Bulgaria yEstados Unidos.
Porúltimo, se aclaró que a partir de la autorización dispuesta “comenzará laimportación, por lo cual se requerirá de un lapso de tiempo para que esténdisponibles en farmacia para su venta”.